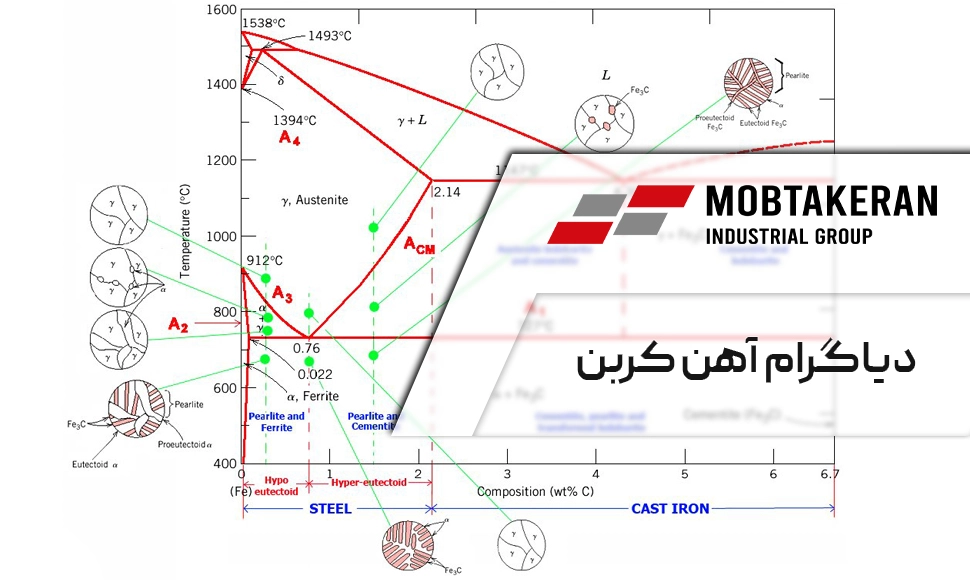
دیاگرام آهن کربن که اصطلاح صحیح آن دیاگرام فازی آهن-کاربید آهن (Fe3C) برشی از دیاگرام فازی آهن کربن (Fe-C) تا غلظت ۶.۶۷ درصد وزنی کربن است که به اشتباه با نام دیاگرام آهن-کربن شناخته شده است. در این مقاله واحد آموزش و مشاوره گروه صنعتی مبتکران کوشیده است دیاگرام فازی آهن کربن را به سادگی بررسی نماید.
آموزش دیاگرام آهن کربن
پیش از آموزش دیاگرام آهن کربن باید گفت که کربن یک عنصر نافلزی است که اغلب به صورت بین نشین در داخل شبکه فلزات قرار گرفته و از طریق تشکیل محلول جامد استحکام آنها را بالا میبرد. یا اینکه با عناصر کاربیدزا واکنش داده و فازهای ثانویه کاربیدی تشکیل خواهد داد که میتوانند از طریق پیرسازی باعث افزایش استحکام آلیاژ شوند.
آهن نیز یک عنصر فلزی است که در دماهای مختلف، ساختارهای بلوری متفاوتی دارد. آهن خالص در دمای اتاق ساختار بلوری BCC دارد. با عبور دما از حدود ۹۱۰ درجه سانتیگراد، ساختار بلوری آهن از BCC به FCC تغییر پیدا میکند. با ادامه افزایش دما و عبور از حدود ۱۴۰۰ درجه سانتیگراد، ساختار بلوری FCC مجددا به BCC تبدیل خواهد شد. در این میان، با قرار گرفتن کربن به شکل بین نشین در داخل هر یک از این ساختارها، محلولهای جامد کربن در آهن تشکیل شده و با نامهای مختلف بر روی نمودار آهن کربن مشخص میشوند.
فازهای تشکیل شده در دیاگرام آهن کربن
محلول جامد کربن در آهن BCC در دماهای پایین، فریت یا فاز α (آلفا) و در دماهای بالاتر از ۱۴۰۰ درجه سانتیگراد، فاز δ (دلتا) نامیده میشود. محلول جامد کربن در آهن FCC که در میان این دو حالت قرار میگیرد، آستنیت یا فاز γ (گاما) نامیده میشود. آهن جزو عناصری محسوب میشود که با کربن واکنش داده و کاربید آهن (Fe3C) تشکیل میدهد که با نام سمنتیت نیز شناخته میشود. این فاز بسته به ترکیب شیمیایی فولاد و غلظت کربن در داخل آهن میتواند در دماهای بالا یا پایین تشکیل شود.
دیاگرام آهن کربن به زبان ساده
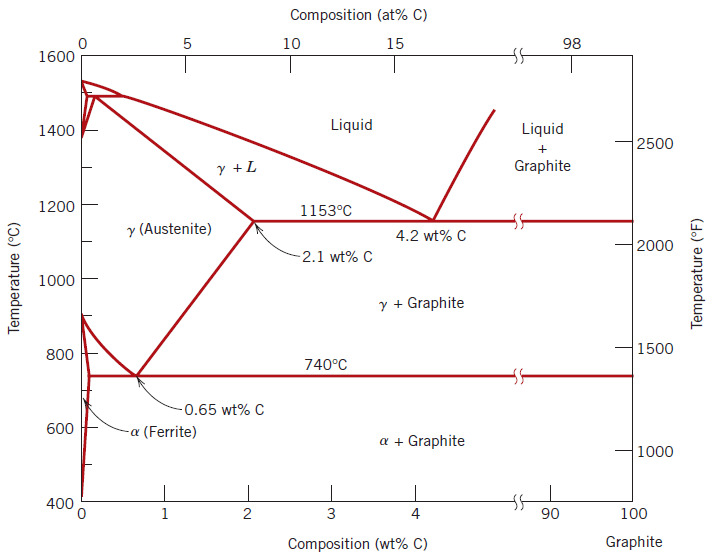
دیاگرام آهن کربن به زبان ساده
بر روی دیاگرام دو نوع منطقه یا ناحیه دیده میشود: مناطق تک فازی و مناطق دو فازی. در مناطق تک فاز که تنها با یک حرف مشخص شدهاند، ساختار فولاد به طور کامل متشکل از همان فاز است. برای مثال، با بالا رفتن دمای یک ساختار فریتی-پرلیتی و وارد شدن به ناحیه γ (آستنیت) و نگهداری به مدت کافی در این منطقه، ساختار فولاد به طور کامل به فاز آستنیت تبدیل خواهد شد. در مقابل، ناحیههایی که با دو فاز نامگذاری شدهاند (مانند α+γ)، در میان دو ناحیه تک فاز (α و γ) قرار گرفته و بیانگر این هستند که ساختار فولاد با قرار گرفتن در این نواحی از این دو فاز تشکیل خواهد شد. درک قانون اهرم به بیان دیاگرام آهن کربن به زبان ساده کمک مینمایید.
قانون اهرم در دیاگرام آهن کربن
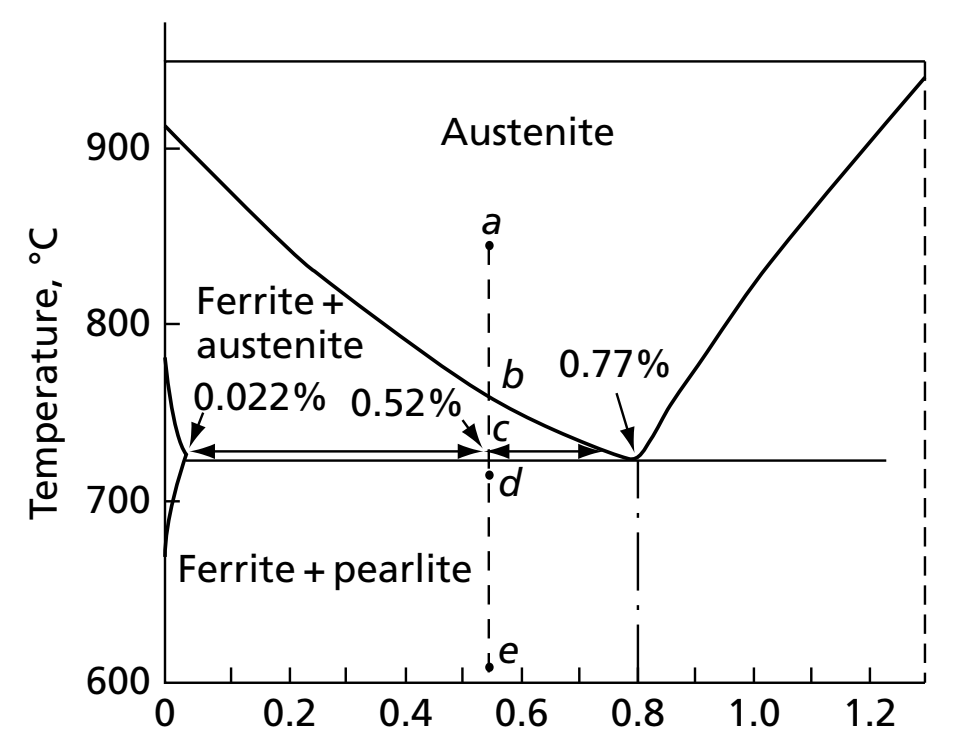
برای محاسبه درصد یا کسر حجمی هر فاز در نواحی دو فازی از قانون اهرم در دیاگرام آهن کربن استفاده میشود. بر این اساس، یک خط افقی در دمای مورد نظر در ناحیه دو فازی رسم میشود که از دو طرف به نواحی تک فاز ختم میشود. در گام بعدی برای محاسبه درصد هر یک از فازها، طول بازوی مخالف را به طول کل خط (اهرم) تقسیم شده و عدد بدست آمده در ۱۰۰ ضرب میشود. به مثال زیر که از کتاب متالورژی فیزیکی ریدهیل آورده شده است، توجه نمایید:
فولادی که حدود ۰.۵۲ درصد وزنی کربن در ساختار خود دارد، پس از آستنیته شدن در دمای بالا به آرامی در راستای خط ae شروع به سرد شدن میکند. با رسیدن به نقطه b و قطع کردن خط مرزی میان ناحیه تک فاز آستنیت و ناحیه دو فازی فریت + آستنیت، فاز فریت در مرز دانههای آستنیت شروع به جوانه زنی کرده و تا رسیدن به نقطه c بر روی خط افقی مربوط به واکنش یوتکتوئید به رشد خود ادامه میدهد. این فاز فریت که پیش از وقوع واکنش یوتکتوئید تشکیل میشود، اصطلاحاً فریت پرویوتکتوئید نامیده میشود. با رسیدن به نقطه c و انجام واکنش یوتکتوئید، تمام آستنیت باقی به مخلوط در هم تنیده از فاز فریت و سمنتیت تبدیل میگردد که محصول واکنش یوتکتوئید بوده و به آن پرلیت گفته میشود. برای محاسبه درصد آستنیت و فریت پرویوتکتوئید درست پیش از وقوع استحاله یوتکتوئید (در نقطه c پیش از انجام واکنش) از قانون اهرم به شکل زیر استفاده میشود:
درصد کربن محلول در فاز فریت بسیار کم بوده و از همین جهت تقریباً معادل با صفر در نظر گرفته میشود. برای محاسبه درصد آستنیت پیش از وقوع واکنش یوتکتوئید، باید طول بازوی مخالف فاز آستنیت (از نقطه c تا جایی که خط افقی به ناحیه تک فاز فریت میرسد-تقریباً صفر) را بر طول کل خط تقسیم کرد. بر این اساس، طول بازوی مخالف بر طول کل خط تقسیم شده و درصد فاز آستنیت برابر ۶۷% محاسبه میشود. بنابراین، ساختار نهایی فولاد، شامل ۳۳% فریت پرویوتکتوئید به همراه ۶۷% آستنیت است که با کاهش دما و انجام واکنش یوتکتوئید تمام آن به پرلیت تبدیل میشود.
یکی از انواع فولادهای یوتکتوئید فولاد ۱.۲۳۴۴ است که به آن H13 نیز گفته می شود و از طریق لینک زیر میتوانید اطلاعات این فولاد را مشاهده نمایید.
نمودار آهن کربن
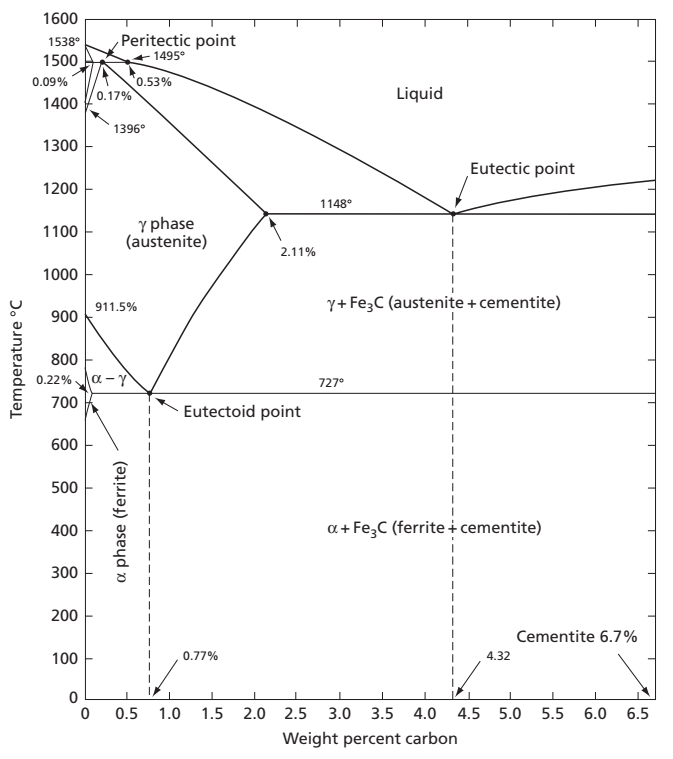
نمودار آهن کربن
سه نوع واکنش در سیستم آلیاژی آهن-کاربید آهن و یا نمودار آهن کربن به وقوع میپیوندد که با خطوط افقی روی نمودار مشخص میشوند.
- واکنش اول که در دمای ℃۱۴۹۵ رخ میدهد، پریتکتیک نام دارد که در آن فاز مذاب با فاز δ واکنش داده و فاز γ (آستنیت) حاوی ۱۷/۰% کربن در نقطه پریتکتیک تشکیل میشود.
- واکنش دوم در نمودار آهن کربن یوتکتیک نام دارد که در دمای ℃۱۱۴۸ رخ داده و بیشتر به چدنها مربوط میشود. در این واکنش، مذاب فولاد حاوی ۳۲/۴% کربن در نقطه یوتکتیک به یک مخلوط در هم تنیده از دو فاز آستنیت و سمنتیت (که لدبوریت نامیده میشود) تبدیل میشود.
- واکنش سوم که در دمای ℃۷۲۷ به وقوع میپیوندد، واکنش یوتکتوئید است که در طی آن فاز آستنیت با ۷۷/۰% وزنی کربن در نقطه یوتکتوئید، به مخلوطی در هم تنیده از دو فاز فریت و سمنتیت (که پرلیت نامیده میشود) تبدیل خواهد شد.
هر یک از فازهای نام برده شده در نمودار آهن کربن، خواص فیزیکی و مکانیکی خاص خود را دارند. با استفاده از انواع عملیات حرارتی که در مقاله عملیات حرارتی به آن اشاره شده است، میتوان ریزساختار فولاد را برای رسیدن به خواص مکانیکی مطلوب و مورد نظر را کنترل نمود.
شایان ذکر است که فازهای نشان داده شده بر روی این نمودار، در واقع فازهای تعادلی سیستم آلیاژی آهن-سمنتیت هستند که بر اثر سرد شدن بسیار آهسته مذاب فولاد در زمانهای طولانی تشکیل میشوند. فازهای دیگری که در طی برخی از عملیات حرارتی و بر اثر سرد شدن سریع ساختار تشکیل میشوند (مانند بینیت و مارتنزیت)، فازهای غیر تعادلی هستند که بر روی نمودار اهن کربن نمایش داده نمیشوند. برای نمایش فازهای غیرتعادلی از دیاگرامهای CCT یا TTT استفاده میشود.
ترکیب آهن و کربن
آلیاژهای آهن-سمنتیت را به طور کلی میتوان به دو گروه فولادها و چدنها تقسیم نمود. فولادها، آلیاژهایی متشکل از آهن و سمنتیت هستند که حداکثر تا ۱/۲% کربن در ترکیب آنها وجود دارد. آلیاژهای آهن با بیش از ۱/۲% کربن نیز چدن نامیده میشوند. فولادها را نیز بر مبنای درصد کربن آنها میتوان به دو گروه هیپویوتکتوئید (درصد کربن کمتر از ۷۷/۰) و هایپریوتکتوئید (درصد کربن بیشتر از ۷۷/۰) تقسیم نمود. این تقسیمبندی بر مبنای درصد کربن در نقطه یوتکتوئید روی نمودار است.